二三类医疗器械注册变更
日期:2019-09-10 / 人气: / 来源: / 编辑:Sasha根据《医疗器械监督管理条例》(国务院令第680号)的规定,对中华人民共和国境内的医疗器械按照风险程度实行分类管理。共分3类,分别是第I类、第II类、第III类。
第Ⅱ类是具有中度风险,需要严格控制管理以保证其安全、有效的医疗器械,境内生产企业需要在所在地省(直辖市)药监局进行注册,境外医疗器械生产企业需要委托境内代理人在国家药监局进行注册。
第Ⅲ类是具有较高风险,需要采取特别措施严格控制管理以保证其安全、有效的医疗器械,无论境内、境外医疗器械生产企业均需要在国家药监局进行注册。
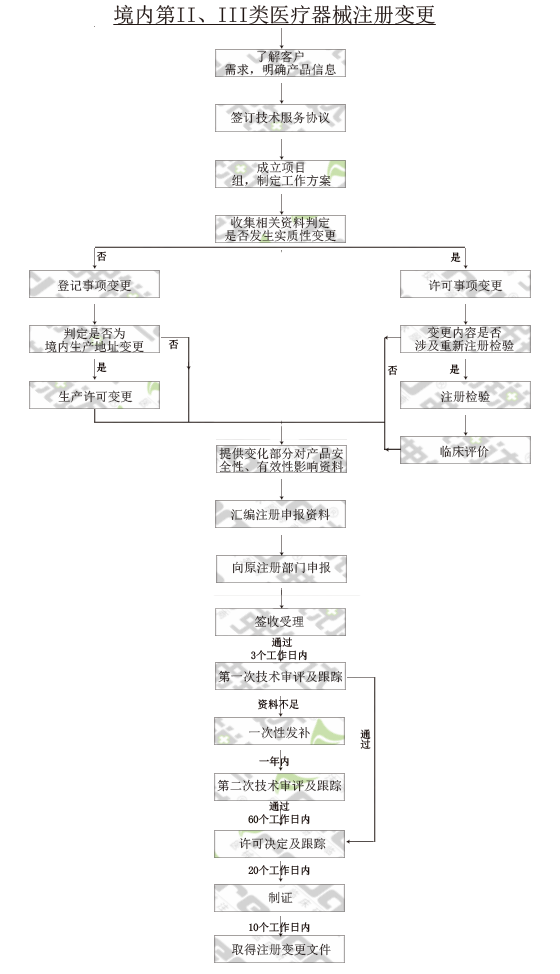
已注册的第二类、第三类医疗器械产品,其设计、原材料、生产工艺、使用范围、使用方法等发生实质性变化,有可能影响该医疗器械安全、有效的,注册人应向原注册部门申请办理变更注册手续;发生非实质性变化,不影响该医疗器械安全、有效的,应当将变化情况向原注册部门备案。
相关法规:
温馨提示,本站部分内容来源网络,如有侵权,请联系删除!

道和思源(北京)科技有限公司成立于2014年,专注于医疗器械法规咨询服务,致力于为客户将安全、有效和合规的医疗器械产品迅速推向并占领全球市场,是中国领先的医疗器械CRO创新服务企业。主要服务项目有:进口一类医疗器械备案、进口二类医疗器械注册、进口三类医疗器械注册、国产三类医疗器械注册、医疗器械软件注册、临床实验、创新医疗器械申报港澳台医疗器械注册等。
TAG:
- 上一篇:二三类医疗器械注册延续
- 下一篇: 北京道和思源科技有限公司医疗器械代办怎么样?
猜你喜欢
- 不得了!朋友圈里发布医疗器械产品或犯法2019-03-13
- 最近两天医疗器械注册热点新闻2018-11-23
- 我国医疗人工智能正加速产业化落地2020-06-28
- 医疗器械延续注册要求解读2019-10-18
- 国家药监局发布各省医疗器械许可备案相关信息(截至2021年12月31日)2022-01-10
- 医疗器械拓展性临床试验管理规定(试行)》解读2020-03-22
- 医疗器械临床试验EDC常见疑问2018-12-28
- 国家药监局关于批准注册73个医疗器械产品的公告(2020年10月)(2020年第128号公告)2020-11-19
- 医疗器械临床试验设计之优效性试验2020-05-27
- 《医疗器械分类目录》子目录01、04、07、08、09、10、19、21相关产品临床评价推荐路径使用说明2022-07-15
- 2020年1月进口第一类医疗器械产品备案信息2020-03-10
- 关于YY1116一2020和YY0167一2020行业标准部分解释2020-03-12
- 国家药监局2019年监管方向已定2019-01-18
- 关于2018年11月-12月医疗器械注册受理前技术问题咨询工作安排的公告(第223号)2018-11-19
- 国家药监局发布2021年08月进口第一类医疗器械产品备案信息2021-09-03
- 【汇总】十八省市防疫相关医疗器械应急审批绿色通道2020-02-11











