国家药监局:这27批(台)医疗器械不合格 涉及手术衣、医用脱脂棉等产品
日期:2020-11-19 / 人气: / 来源: / 编辑:Sasha11月17日,国家药监局网站发布国家药监局关于发布国家医疗器械监督抽检结果的通告(第4号)(2020年第74号),内容如下。
国家药监局关于发布国家医疗器械监督抽检结果的通告(第4号)(2020年第74号)
发布时间:2020-11-17
为加强医疗器械质量监督管理,保障医疗器械产品使用安全有效,国家药品监督管理局组织对半导体激光治疗机、超声洁牙设备、手术衣等5个品种的产品进行了质量监督抽检,共27批(台)产品不符合标准规定。具体情况通告如下:
一、被抽检项目不符合标准规定的医疗器械产品
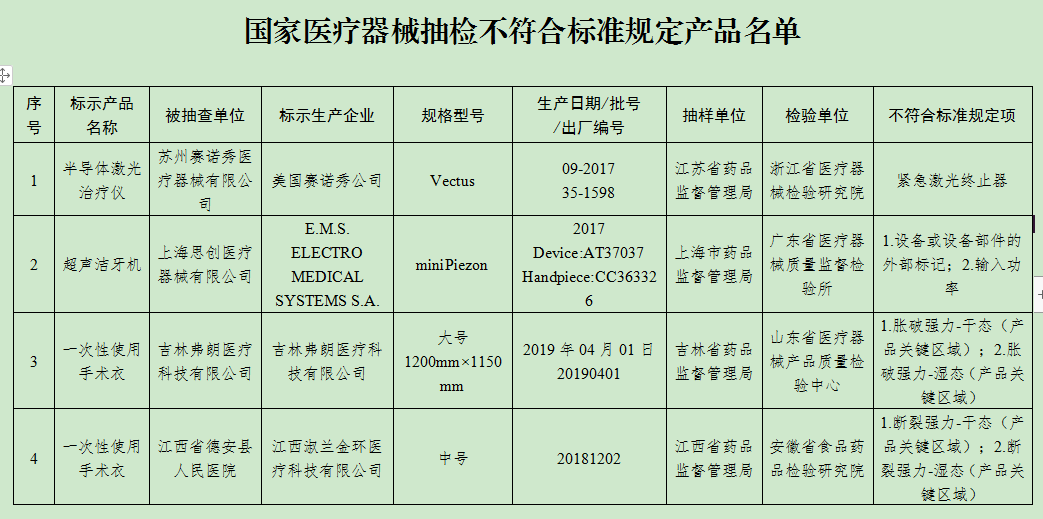
(一)半导体激光治疗机1台产品:美国赛诺秀公司生产,涉及紧急激光终止器不符合标准规定。
(二)超声洁牙设备1台产品:E.M.S. ELECTRO MEDICAL SYSTEMS S.A.生产,涉及设备或设备部件的外部标记、输入功率不符合标准规定。
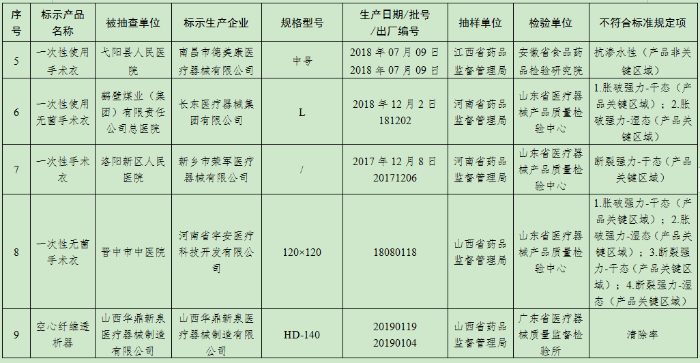
(三)手术衣6批次产品:吉林弗朗医疗科技有限公司、江西淑兰金环医疗科技有限公司、南昌市德美康医疗器械有限公司、长东医疗器械集团有限公司、新乡市荣军医疗器械有限公司、河南省宇安医疗科技开发有限公司生产,涉及胀破强力-干态(产品关键区域)、胀破强力-湿态(产品关键区域)、断裂强力-干态(产品关键区域)、断裂强力-湿态(产品关键区域)、抗渗水性(产品非关键区域)不符合标准规定。
(四)血液透析器1批次产品:山西华鼎新泉医疗器械制造有限公司生产,涉及清除率不符合标准规定。
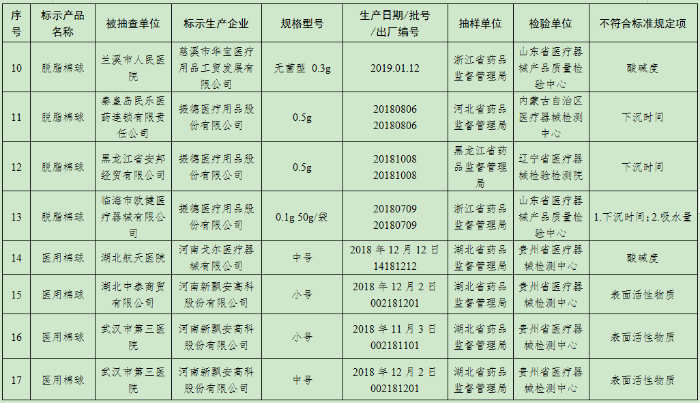
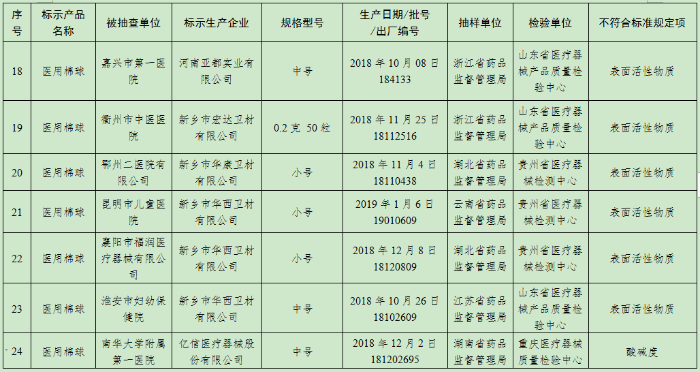
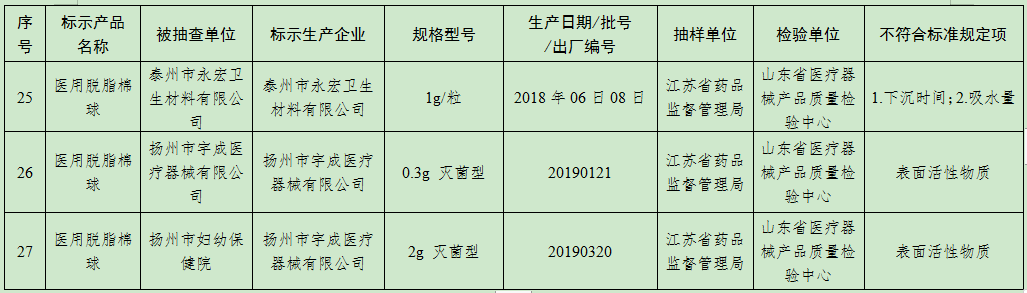
(五)医用脱脂棉18批次产品:慈溪市华宝医疗用品工贸发展有限公司、振德医疗用品股份有限公司、河南戈尔医疗器械有限公司、河南新飘安高科股份有限公司、河南亚都实业有限公司、新乡市宏达卫材有限公司、新乡市华康卫材有限公司、新乡市华西卫材有限公司、亿信医疗器械股份有限公司、泰州市永宏卫生材料有限公司、扬州市宇成医疗器械有限公司生产,涉及酸碱度、下沉时间、吸水量、表面活性物质不符合标准规定。
以上抽检不符合标准规定产品具体情况见附件。
二、对上述抽检中发现的不符合标准规定产品,国家药品监督管理局已要求企业所在地省级药品监督管理部门按照《医疗器械监督管理条例》《医疗器械生产监督管理办法》和《医疗器械召回管理办法》等法规规章要求,及时作出行政处理决定并向社会公布。企业所在地省级药品监督管理部门要督促相关企业对抽检不符合标准规定的产品进行风险评估,根据医疗器械缺陷的严重程度确定召回级别,主动召回产品并公开召回信息;督促企业尽快查明产品不合格原因,制定整改措施并按期整改到位。
特此通告。
附件:国家医疗器械抽检不符合标准规定产品名单
国家药监局
2020年11月13日
温馨提示,本站部分内容来源网络,如有侵权,请联系删除!

道和思源(北京)科技有限公司成立于2014年,专注于医疗器械法规咨询服务,致力于为客户将安全、有效和合规的医疗器械产品迅速推向并占领全球市场,是中国领先的医疗器械CRO创新服务企业。主要服务项目有:进口一类医疗器械备案、进口二类医疗器械注册、进口三类医疗器械注册、国产三类医疗器械注册、医疗器械软件注册、临床实验、创新医疗器械申报港澳台医疗器械注册等。
猜你喜欢
- 甘肃开展全省医疗器械检查员暨企业质量管理能力提升培训2020-11-19
- 植入性医疗器械如何与磁共振兼容2020-07-28
- 江西新闻客户端:江西医疗器械产业加速崛起2020-09-28
- 江苏省药监局全面完成医用防护服医用口罩应急审批2020-07-16
- 天津市市场监管管理委员会关于发布天津市食品经营者食品安全主体责任清单的通告2020-07-14
- 天津市药品监督管理局关于暂停天津市博爱生物药业有限公司生产的通告2020-07-14
- 甘肃举办全省医疗器械临床试验质量管理规范(GCP)暨检查员培训班2020-07-16
- 医疗器械临床评价豁免政策解读 —— 以 2025 年目录为例2025-05-14
- 甘肃召开碳离子治疗系统重点监测工作启动暨专家研讨会2020-10-30
- 河北省药品监督管理局印发《关于支持医疗器械经营环节创新发展的有关政策措施》的通知2020-09-18
- 新疆维吾尔自治区吐鲁番市开展医疗器械安全宣传周活动2020-10-26
- 登革病毒核酸检测试剂注册审评概述2020-11-20
- 医疗器械注册申请批件领取通知2020-09-08
- 天津市食品安全检测技术研究院2020年公开招聘高层次人才工作方案2020-09-15
- 新型冠状病毒诊断试剂国家标准送审稿讨论会在京召开2020-11-09
- 2025 年免于临床评价医疗器械之手术器械篇2025-05-14











