国产二类医疗器械注册/延续/变更/收费标准
日期:2021-03-31 / 人气:

道和思源是国内一流的医疗器械产品注册代理公司,我们的技术团队深谙医疗器械注册的相关法规,秉承着对客户负责任为信念,在充分了解客户需求的前提下,为客户提供最专业、最高效的服务。
二类医疗器械注册过程中,道和思源能为您提供
1、产品分类界定、注册咨询;
2、GMP质量管理体系建设与规划辅导;
3、产品技术要求、说明书及标签编写辅导与审核;
4、型式检验样品要求、检测机构确认及检验过程跟踪协调;
5、产品临床评价、临床策划、临床试验审批、试验实施、临床统计。
6、各类注册技术文档编制;
7、注册申请与注册技术审评跟踪协调;
8、质量体系模拟考核与现场考核辅导;
9、其他相关注册咨询服务。
国产二类医疗器械注册变更
根据《医疗器械监督管理条例》(国务院令第650号)的规定,对中华人民共和国境内的医疗器械按照风险程度实行分类管理。共分3类,分别是第I类、第II类、第III类。
第Ⅱ类是具有中度风险,需要严格控制管理以保证其安全、有效的医疗器械,境内生产企业需要在所在地省(直辖市)药监局进行注册,境外医疗器械生产企业需要委托境内代理人在国家药监局进行注册。
已注册的第二类医疗器械产品,其设计、原材料、生产工艺、使用范围、使用方法等发生实质性变化,有可能影响该医疗器械安全、有效的,注册人应向原注册部门申请办理变更注册手续;发生非实质性变化,不影响该医疗器械安全、有效的,应当将变化情况向原注册部门备案。

国产二类医疗器械变更流程图
国产二类医疗器械变更相关法律法规
1、《医疗器械监督管理条例》(国务院令第650号)
2、《医疗器械注册管理办法》(局令第4号)
3、《医疗器械分类规则》(局令第15号)
4、《医疗器械分类目录》(2018)
5、《医疗器械说明书和标签管理规定》(局令第6号)
6、《医疗器械临床试验质量管理规范》(局令第25号)
7、《医疗器械生产质量管理规范》(2014年 第64号)
8、《医疗器械生产监督管理办法》(局令第7号)
9、《境内第三类医疗器械注册质量管理体系核查工作程序(暂行)》(食药监械管〔2015〕63号)
10、《国产第三类医疗器械变更注册审批服务指南》
国产二类医疗器械延续注册
根据《医疗器械监督管理条例》(国务院令第650号)的规定,对中华人民共和国境内的医疗器械按照风险程度实行分类管理。共分3类,分别是第I类、第II类。
第Ⅱ类是具有中度风险,需要严格控制管理以保证其安全、有效的医疗器械,境内生产企业需要在所在地省(直辖市)药监局进行注册,境外医疗器械生产企业需要委托境内代理人在国家药监局进行注册。
医疗器械注册证有效期届满需要延续注册的,注册人应当在医疗器械注册证有效期届满6个月前,向食品药品监督管理部门申请延续注册。

国产二类医疗器械延续注册流程图
国产二类医疗器械延续注册相关法律法规
1、《医疗器械监督管理条例》(国务院令第650号)
2、《医疗器械注册管理办法》(局令第4号)
3、《医疗器械分类规则》(局令第15号)
4、《医疗器械分类目录》(2018)
5、《医疗器械说明书和标签管理规定》(局令第6号)
6、《医疗器械临床试验质量管理规范》(局令第25号)
7、《医疗器械生产质量管理规范》(2014年 第64号)
8、《医疗器械生产监督管理办法》(局令第7号)
9、《境内第三类医疗器械注册质量管理体系核查工作程序(暂行)》(食药监械管〔2015〕63号)
10、《国产第三类医疗器械延续注册审批服务指南》
国产二类医疗器械注册参考费用
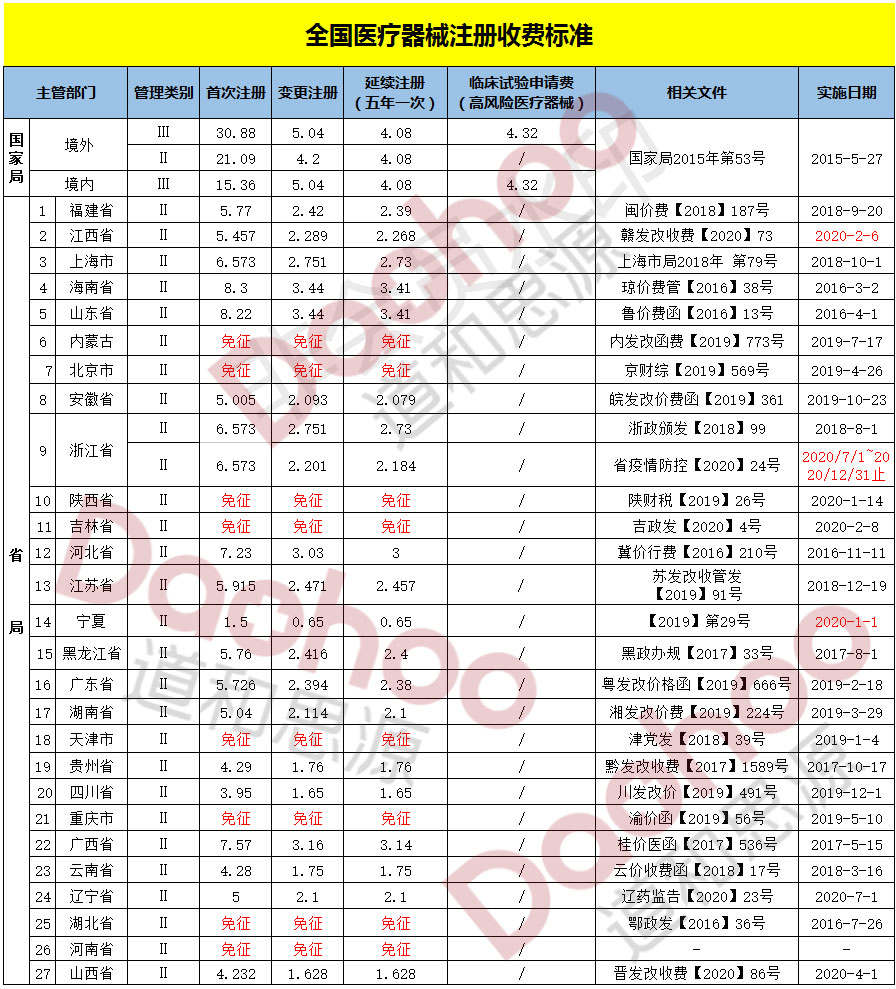
此项服务根据客户的需求定制注册方案,因产品不同、目的不同,研究复杂程度及规模差异很大,请留下您的联系方式,或直接拨打电话13521090701。
国产二类医疗器械注册服务流程图
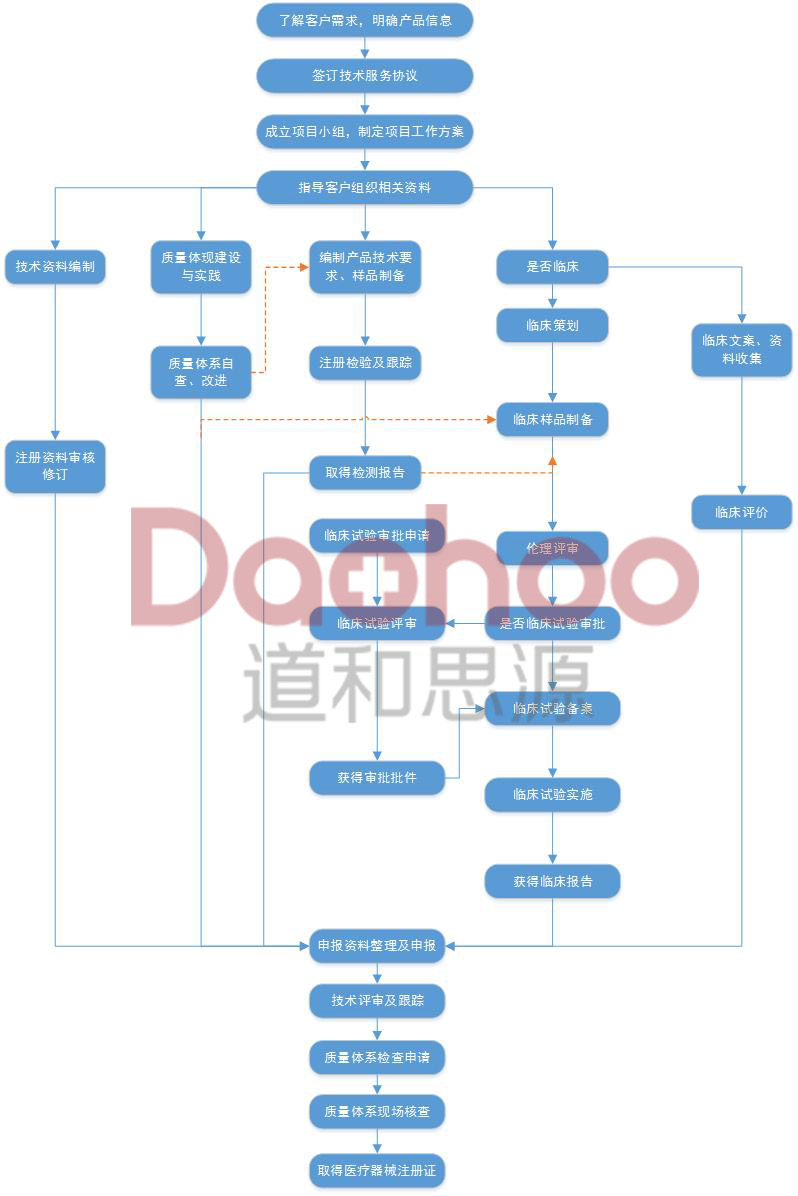

医疗器械软件合规上市,我们更快
快速响应、专业系统、快速行动、高效上市,道和思源首创的X7提速体系,使每个项目平均省时60天。

道和思源历史通过率100%
在全球服务的100+项目中,通过率100%。选择我们,就等于选择了竞争优势。

全程168步省心服务优化
关于于医疗器械软件合规上市相关法规、政策,我们更专业。关于合规上市的客户服务,我们更用心。
-
上一篇:暂无
- 下一篇: 进口二类医疗器械注册/延续/变更/收费标准










