天津第二类医疗器械说明书变更备案
基本信息
| 事项名称 | 第二类医疗器械说明书变更备案 | 事项类型 | 其他行政权力 |
|---|---|---|---|
| 办理部门 | 天津市药品监督管理局 | 主管部门 | 天津市药品监督管理局 |
| 法定办理时限 | 20个工作日查看说明 | 承诺办理时限 | 4个工作日查看说明 |
| 是否涉及特殊环节 | 无; | 受理时间 | 周一至周五工作日上午:9:00 至 11:30下午:13:30 至 17:00 |
| 是否马上办 | 是 | 业务主管部门 | 天津市药品监督管理局 |
| 办理部门 | 天津市药品监督管理局 | 实施编码 | 11120000MB1662153N3121031026000 |
| 咨询电话 |
022-23520832 |
监督电话 | 投诉电话:83555385 地址:南开区红旗南路237号 |
| 办理地点 |
南开区红旗南路237号 |
通办范围 | 跨区 |
| 有效期限 | 与对应的第二类医疗器械注册证书有效期限相同 | 适用范围 | 全省 |
| 是否预约审批 | 否 | 预约审批电话 | -- |
| 到现场办事次数 | 1 | 权力来源 | 法定机关 |
| 是否网上办事项 | 是 | 是否就近办事项 | 是 |
| 是否一次办事项 | 是 | 是否无人审批事项 | 否 |
| 是否承诺审批事项 | 否 | 是否以函代办事项 | 否 |
| 是否同城通办事项 | 是 | 办件公示 | 否 |
| 监管细则 | 32第二类医疗器械说明书变更备案事项监管细则.docx | ||
| 审批收费 | |||
| 是否收费 | 否 | ||
| 收费标准 | 不涉及 | ||
| 实施权限 | |||
| 市级权限 | 本市行政区域内的申请,由天津市市场监督管理委员会(市药品监督管理局)办理 | ||
| 自贸试验区权限 | 本行政区域内,不应有此权限 | ||
| 滨海新区权限 | 本行政区域内,不应有此权限 | ||
| 市区权限 | 本行政区域内,不应有此权限 | ||
| 郊区权限 | 本行政区域内,不应有此权限 | ||
办理形式
| 运行系统 | 县级 | 系统名称 | 天津市医疗器械企业服务平台 |
|---|---|---|---|
| 是否支持网上支付 | 否 | 是否支持物流快递 | 否 |
| 预约途径 | 无 | 办理类型 | 承诺件 |
| 是否数量限制 | 否 | ||
| 是否联办 | 否 | 联办部门 | -- |
申请条件
a)已取得第二类医疗器械注册证书;
b)已注册的医疗器械发生注册变更的,申请人应当在取得变更文件后,依据变更文件自行修改说明书和标签。说明书的其他内容发生变化的,应当向医疗器械注册的审批部门书面告知。
办理依据
| 序列 | 法律名称 | 条数 | 附件 |
| 1 | 《医疗器械说明书和标签管理规定》(国家食品药品监督管理总局第6号令,2014年) | 第16条 | 《医疗器械说明书和标签管理规定》(国家食品药品监督管理总局第6号令,2014年) |
其他依据
申请材料
| 序号 | 材料名称 | 材料形式 | 材料要求 | 材料下载 | 其他信息 |
| 1 | 天津市第二类医疗器械注册证说明书更改告知书 |
原件:0 复印件:1 纸质 |
主审材料 材料准备要点 其他要求 |
天津市第二类医疗器械注册证说明书更改告知书.doc 天津市第二类医疗器械注册证说明书更改告知书及填写说明.doc |
材料来源 |
| 2 | 申报注册时所提交说明书的复本 |
原件:0 复印件:1 纸质 |
主审材料 材料准备要点 其他要求 |
材料来源 |
|
| 3 | 更改备案的说明书 |
原件:0 复印件:1 纸质 |
主审材料 材料准备要点 其他要求 |
材料来源 |
收费项目信息
不收费
中介服务
无
办理流程
| 序号 | 流程 | 详细内容 | ||
| 1 | 受理 |
| 环节名称 | 形式审查 |
| 审查标准 | 天津市第二类医疗器械注册证说明书更改告知书 应主要审查以下内容: 所填写项目应齐全、准确,更改前后情况清晰、明确; 申报注册时所提交说明书的复本 应主要审查以下内容: 确保说明书版本正确; 更改备案的说明书 应主要审查以下内容: 确保更改后的说明书格式符合《医疗器械说明书和标签管理规定》(国家食品药品监督管理总局第6号令)。更改内容不涉及医疗器械注册许可事项变更和登记事项变更内容,且与产品实际相符。 |
| 结果 | 接件人员根据下列情况分别作出处理: a)申请材料齐全、符合法定形式,或者申请人按照办理部门的要求提交全部补正申请材料的,应当在天津网上办事大厅或“天津市医疗器械企业服务平台”上,受理该申请,并出具《受理告知书》; b)申请事项依法不需要办理的,应当即时告知申请人不受理,并出具《不予受理告知书》。 |
| 2 | 审查 |
| 环节名称 | 纸质审查 |
| 审查标准 | 纸质审查主要审查以下内容: c)格式正确; d)内容合法; e)按照法律法规规定查验原件与复印件的一致性 |
| 结果 | 通过/不予通过 |
| 3 | 决定 |
| 环节名称 | 决定 |
| 审查标准 | 依据申请条件作出决定 |
| 结果 | 办理工作人员应根据法律、法规、规章和审查意见,并按照下列情况分别作出处理: a)申请人提交的申请材料齐全、符合法定形式的,应在承诺时限内办理完成,并予以备案; b)网上办理事项申请材料齐全、符合法定形式的,予以备案; c)通过智能终端进行申请办理的,当场出具有关决定; d)依法作出不予办理的,应当说明理由,并告知申请人享有依法申请行政复议或者提起行政诉讼的权利。 |
流程图
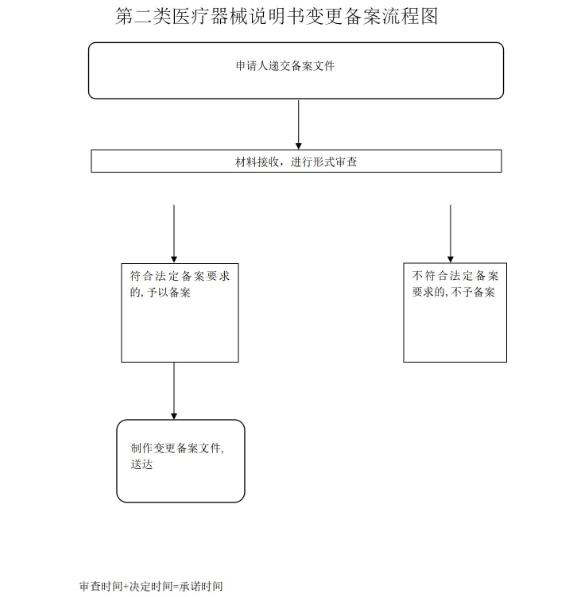
办理结果
| 序列 | 结果名称 | 结果样板 |
| 1 | 《天津市第二类医疗器械注册证说明书更改告知书》 | 无 |

