办理二类医疗器械注册证(二类医疗器械注册证办理注意事项)
办理二类医疗器械注册证,二类医疗器械注册证办理注意事项。本文通过北京药监局二类医疗器械注册证办理规定围绕这个问题详细的跟大家说说。
医疗器械注册证是干嘛的?(了解这个知识点的可以直接pass过去)
医疗器械注册,是指依照法定程序,对拟上市销售、使用的医疗器械的安全性、有效性进行系统评价,以决定是否同意其销售、使用的过程。它分为境内医疗器械注册和境外医疗器械注册,境外的医疗器械不管是一类,二类,三类都要到北京国家食品药品监督局办理:境内的一,二类医疗器械在当地的省或市食品药品监督局办理,三类的到国家食品药品监督局办理。医疗器械注册证是指医疗器械产品的合法身份证。

一、办理二类医疗器械注册证需要准备的文件
1、境内医疗器械注册申请表;
2、资格证明:
包括营业执照副本,并且所申请产品应当在生产企业许可证核定的生产范围之内;
3、产品技术要求:
至少应当包括技术指标或者主要性能要求的确定依据等内容;
4、安全风险分析报告:
按照YY0316《医疗器械风险分析》标准的要求编制。应当有能量危害、生物学危害、环境危害、有关使用的危害和由功能失效、维护不周及老化引起的危害等五个方面的分析以及相应的防范措施;
5、适用的产品标准及说明:
采用国家标准、行业标准作为产品的适用标准的,应当提交所采纳的国家标准、行业标准的文本;注册产品标准应当由生产企业签章。生产企业应当提供所申请产品符合国家标准、行业标准的声明,生产企业承担产品上市后的质量责任的声明以及有关产品型号、规格划分的说明;
6、产品性能自测报告:
产品性能自测项目为注册产品标准中规定的出厂检测项目,应当有主检人或者主检负责人、审核人签字。执行国家标准、行业标准的,生产企业应当补充自定的出厂检测项目;
7、医疗器械检测机构出具的产品注册检测报告:
需要进行临床试验的医疗器械,应当提交临床试验开始前半年内由医疗器械检测机构出具的检测报告。不需要进行临床试验的医疗器械,应当提交注册受理前1年内由医疗器械检测机构出具的检测报告。
8、医疗器械临床试验资料;(如需)
9、医疗器械说明书;
申请人提交的医疗器械说明书应当符合《医疗器械说明书、标签和包装标识管理规定》。
10、产品生产质量体系考核(认证)的有效证明文件——根据对不同产品的要求,提供相应的质量体系考核报告:
①省(食品)药品监督管理部门签章的、在有效期之内的质量体系考核报告;
②医疗器械生产质量管理规范检查报告或者医疗器械质量体系认证证书;
③国家已经实施生产实施细则的,提交实施细则检查验收报告;
11、申请人应当对其所提交材料真实性的自我保证声明:
应当包括所提交材料的清单、生产企业承担法律责任的承诺。
12、申请人不是法定代表人或负责人本人,企业应当提交《授权委托书》2份;
13、按申请材料顺序制作目录,如需提交软盘的,一并提交有效的软盘资料。
注:
①申请材料完整、清晰,签字并加盖企业公章。使用A4纸打印或复印按照申请材料目录顺序装订成册。
②凡申请材料需提交复印件的,申请人(单位)须在复印件上注明“此复印件与原件相符”字样或者文字说明,注明日期,加盖单位公章。
二、办理二类医疗器械注册证需要多长时间
1、产品立项至检测阶段
预计4-7个月,不含开发过程时间(并行)。
2、临床阶段
如需临床预计6个月以上1年左右,视产品而定。
3、申报注册阶段
申报注册全过程预算8个月。(158工日,20工日/月,不计节假),体考时间(并行),不含整改、资料发补耗时。
发补时限0~12个月,考虑平均时间6个月。视产品首次申报资料情况而定。
体系考核:在受理后10工作日内申请体系考核。1个月内完成体系考核。考核及整改不通过,即退审。
体系整改:根据体系考核整改程度,分为
(a)1个月整改期,结束后继续一次审评阶段。
(b)6个月整改期,结束后进入二次审评阶段。
体系考核、体系整改时间与技术审评阶段并行。
4、正常预算合计(具体情况请具体分析)
不含临床周期,预计在1年左右;
含临床周期,预计在1年半到3年左右,甚至更长。
三、办理二类医疗器械注册证需要多少钱
1、官方收费看下图,部分地区收费标准可能有所变动,收费标准以当时收费情况而定。该收费不包含临床费用以及其他检测费用和代理费用。
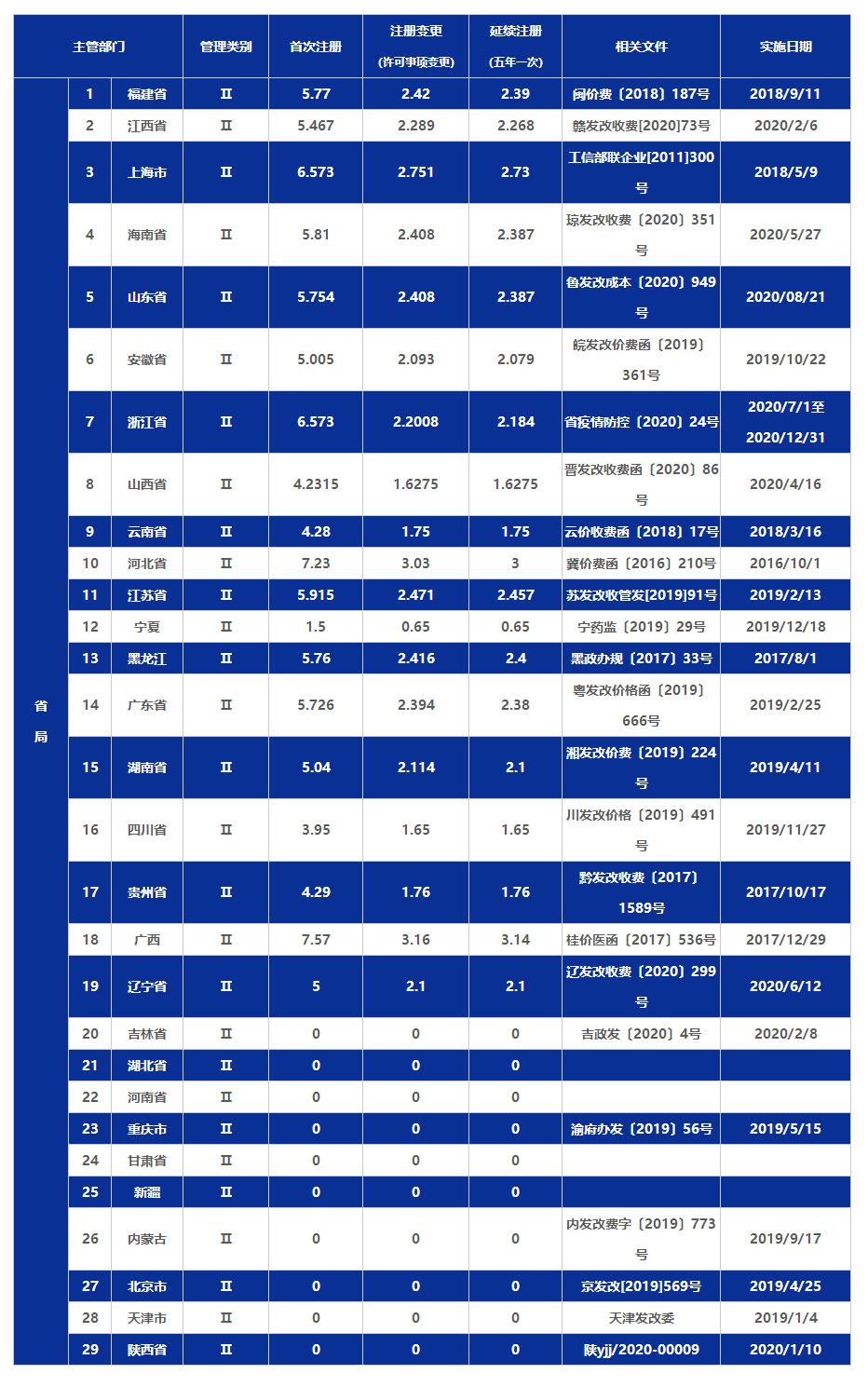
2、中介收费,根据产品具体情况而定,详细报价可直接联系李经理13521090701(微信同号)
四、软件二类医疗器械注册证办理有没有区别和其他要求
因为医疗器械软件是属于医疗器械的,所以医疗器械软件办理二类医疗器械注册证没有根本性的要求,只要按照对应的标准以及指导原则基本上就完事,但这里需要提醒的是,医疗器械软件是分为独立软件和软件组件,其中独立软件是可以直接按照医疗器械注册申报,而软件组件只能和配套的医疗器械一起注册申报才行。
好了,本文关于办理二类医疗器械注册证,二类医疗器械注册证办理注意事项。就分想到这里,希望本篇文章能帮到您,如果还有什么不解的,可以直接联系我们。

