国家药监局发布广东吉华医疗器械有限公司对一次性使用医用口罩信息
索引号:JGXX-2021-10001
主题分类:监管信息 / 责令召回信息
标题:广东吉华医疗器械有限公司对一次性使用医用口罩[儿童型](疫情应急产品)主动召回
发布日期:2021-09-24
广东吉华医疗器械有限公司对一次性使用医用口罩[儿童型](疫情应急产品)主动召回
广东吉华医疗器械有限公司生产的一次性使用医用口罩[儿童型],批号为020406-6,经抽检发现不符合标准规定,广东吉华医疗器械有限公司决定发起主动召回。
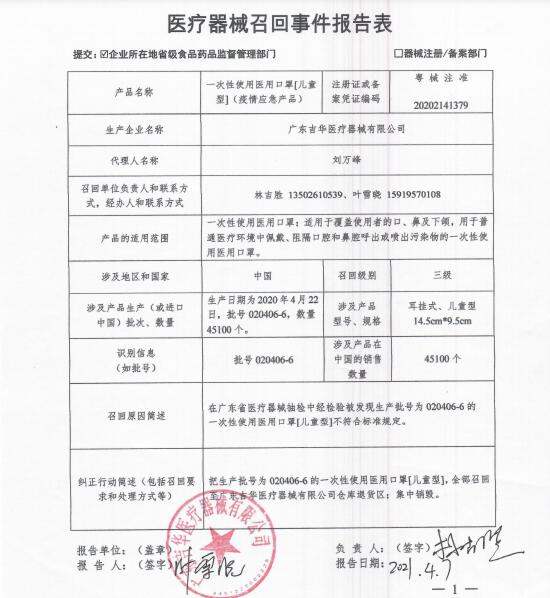
广东吉华医疗器械有限公司对其生产的一次性使用医用口罩[儿童型](注册证号:粤械注准20202141379)批号为020406-6主动召回。召回级别为 三级 。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。
附件:广东吉华-召回事件报告表.pdf
2021年9月22日
公司信息
广东吉华医疗器械有限公司成立于2019年03月13日,注册地位于饶平县钱东紫云村原老蔴厂(德盛毛织服装厂内),法定代表人为林沛。经营范围包括生产、销售:医疗器械、熔喷布、无纺布、口罩配件、劳保用品;货物、技术进出口。(依法须经批准的项目,经相关部门批准后方可开展经营活动)

