病理影像信息传输处理软件属于几类医疗器械,怎么办理注册备案
病理影像信息传输处理软件属于几类医疗器械?根据我在国家药监局数据库查询得到同类名称的产品是属于第二类医疗器械。
 来源:国家药监局
来源:国家药监局
既然知道病理影像信息传输处理软件是第二类医疗期器械了,那就要考虑如何去做第二类医疗器械注册证申请。那么怎么办理第二类医疗器械的注册备案呢?请看下文:
一、二类医疗器械注册证受理条件
已按照有关规定取得企业工商登记。已确定申报产品为第二类医疗器械,已编制完成拟申请产品的医疗器械产品技术要求,并已通过预评价已具备拟注册产品的生产能力;已按照《医疗器械生产质量管理规范》的要求建立医疗器械生产质量管理体系。已取得医疗器械检测机构出具的医疗器械检测报告。办理医疗器械注册申请的人员具有相应的专业知识,熟悉医疗器械注册管理的法规、规章和有关的技术要求。
二、二类医疗器械注册证(首次注册)申请材料要求
1、境内医疗器械注册申请表;
2、资格证明;
3、产品技术要求;
4、安全风险分析报告;
5、适用的产品标准及说明;
6、产品性能自测报告;
7、医疗器械检测机构出具的产品注册检测报告;
8、医疗器械临床试验资料;(如需)
9、医疗器械说明书;
10、产品生产质量体系考核(认证)的有效证明文件——根据对不同产品的要求,提供相应的质量体系考核报告;
11、申请人应当对其所提交材料真实性的自我保证声明;
12、申请人不是法定代表人或负责人本人,企业应当提交《授权委托书》2份;
13、按申请材料顺序制作目录,如需提交软盘的,一并提交有效的软盘资料。
以上基本上是材料的要求,如果觉得申报注册很麻烦,也可以选择专业的CRO公司进行代理注册。
三、二类医疗器械注册证办理流程图
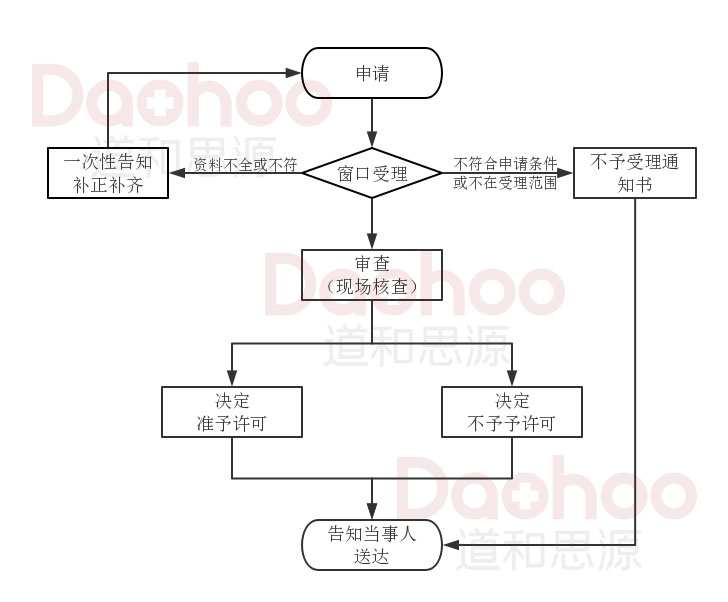
二类医疗器械注册证办理流程图

