袜型医用压力带医疗器械产品注册证申报代办
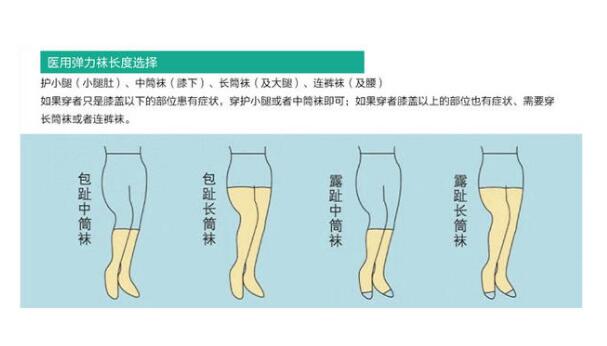
日期:2020-07 / 人气:157袜型医用压力带医疗器械产品是一种经特殊设计,主要用于预防下肢静脉血栓形成,或者缓解下肢静脉曲张症状的医疗器械产品。其科学原理是借助于专门的压力梯度设计,即由脚踝处渐次向上递减,收缩小腿肌肉以对血管腔加压,促使静脉血液回流心脏,防止下肢静脉淤血,确保下肢静脉血液的良好循环,缓解患肢沉重、腿部肿胀等症状。
袜型医用压力带产品的医疗器械注册申报资料要求包含的内容如下:
(一)产品注册单元划分
原则上,按照袜型医用压力带产品的主要原材料、压力等级、预期用途划分为不同注册单元。
(二)综述资料
综述资料应详细论述产品的设计开发、生产控制、货架寿命,以及相关验证内容,所提交的资料应完整、标题明确、目录清晰并具有系统性,至少应包括以下内容:
1.概述
应概述袜型医用压力带境内及原产国(适用于进口产品)的管理类别、分类编码、名称的确定依据等信息。
2.产品描述
医疗器械注册代理应包括产品的压缩力等级、结构组成、图示(标明各组成名称)、工作原理、制造原材料(使用国际通用规范化学名称)、产品的主要功能、交付状态等内容。产品如有区别于其他同类产品的特征也应加以描述。在结构组成项对各组成成分比例,是否染色以及是否重复使用,如何清洁保养,使用寿命进行说明。应明确此类产品不能直接接触破损皮肤表面。
3.规格型号
应从结构组成、原材料、功能、产品特征、性能指标、包装等方面详细列表说明各型号规格间的区别。应采用对比表及带有说明性文字的图片、图表对各种规格型号的不同之处加以区别。
4.包装说明
应说明包装的相关信息,至少包括初包装材料、包装方法、产品在包装中的形态等内容。
5.预期用途和禁忌证
医疗器械产品注册代理预期用途的表述应客观、清晰,使用有明确定义或有行业内公认的术语或名词。描述内容应包括产品压力等级、用于静脉曲张和静脉血栓的症状缓解、适用人群(如持久站立者、孕妇)、产品为可重复使用。
禁忌证应包括该器械不适用的疾病、情况及特定的人群。如对产品材质过敏者、本产品不直接用于破损皮肤表面。
6.与参考产品的对比
医疗器械注册申请应综述参考产品国内外研究及临床使用现状及发展趋势。描述本次申报器械与国内外参考产品的相似点和不同点,建议以列表方式表述,比较的项目应包括产品名称、结构组成、工作原理、预期用途、产品设计、原材料信息、针织工艺、性能指标、有效期、已上市国家等。参考产品应符合本指导原则的定义范畴,可包括本企业或其他企业已上市同类产品,建议采用目前应用较为广泛的产品。
(三)研究资料
产品的研究资料应当从技术层面论述所申报产品的预期用途、设计、技术特征、产品性能指标及制订依据、生物安全性、产品包装验证、产品有效期验证等,对产品所应达到的安全性及有效性给予资料支持。该部分资料应标题明确,目录清晰。至少应包含如下内容:
1.产品性能研究
医疗器械产品注册应提交产品性能的研究资料以及产品技术要求的研究和编制说明,主要包括产品技术要求内容和说明书中所宣称的物理性能、化学性能、生物性能以及与质量控制相关的其他方面的指标要求、采用标准及试验方法的理论基础或实施依据。如何实现“循序阶段压力递减”的原理,请企业提交原材料选择、针织物物理性能与压力关系研究等相关技术资料;提供压力值的设定依据。产品的性能要求及试验方法可参考YY/T 0851-2011《医用防血栓袜》(本指导原则中采用标准适用最新版本,下同)和YY/T 0853-2011《医用静脉曲张压缩袜》进行制定。若未采用YY/T 0851和YY/T 0853中给出的试验方法,应提供所使用的试验方法的来源依据或方法学验证资料。
医疗器械注册代理对于采用新材料制造的产品以及具有其他特殊性能的产品,需根据产品特点制定相应的性能指标和试验方法,应提供性能要求的制定依据或理由、试验方法的来源或方法学验证资料。
产品技术要求编制说明还包括以下内容:
引用或参考的相关标准及资料;
产品概述及主要技术条款确定的依据;
其他需要说明的内容。
2.生物相容性评价研究
医疗器械产品注册代理袜型医用压力带应根据与人体的接触部位、接触方式及接触时间,依据GB/T 16886.1-2011《医疗器械生物学评价第1部分:风险管理过程中的评价与试验》进行生物相容性评价。该产品接触类型为与完整皮肤持久接触(>30天)的表面器械。
研究资料还应包括:生物相容性评价的依据和方法,实施或豁免生物学试验的理由和论证,以及对现有数据或试验结果的评价。应提供关于颜料或染色剂的相关资料,对其是否具有生物相容性进行说明。
3.生物安全性研究
产品若涉及生物安全性研究项目,应按照《国家食品药品监督管理总局关于公布医疗器械注册申报资料要求和批准证明文件格式的公告》(2014年第43号)附件4第五条第(三)款规定提供相应资料。
4.医疗器械产品注册证申请产品有效期和包装研究
产品货架有效期是指产品在一定的温度、湿度、光线等条件的影响下保持其物理、化学、生物学性质的期限。有效期的研究应贯穿于产品研究与开发的全过程,在产品上市后还应继续进行有效期的研究。
货架有效期包括产品有效期和包装有效期。产品有效期验证可采用加速老化或实时老化的研究,实时老化的研究是唯一能够反映产品在规定储存条件下实际稳定性要求的方法。对于包装的有效期验证,建议提交在选择恰当的材料和包装形式,并检测合格后的最终成品包装的初始完整性和维持完整性的检测结果。
在进行加速老化试验研究时应注意:产品选择的环境条件的老化机制应与宣称的贮存、运输环境条件下产品老化的机制相匹配,不应相背离。加速老化研究试验的具体要求可参考YY/T 0681.1。
产品包装验证可依据有关国内、国际标准进行(如GB/T 19633、ISO 11607、ASTM D-4169等),提交产品的包装验证报告,其包装验证的资料内容应与包装说明中给出的信息相符。
5.原材料控制资料
应逐一列明产品生产过程中由起始原料至终产品过程中所需全部材料的化学名称、商品名/材料代号、CAS号、化学结构式/分子式、分子量及分子量分布、使用量、供应商名称、符合的标准等基本信息,建议以列表的形式提供。
医疗器械注册证申请说明原材料的选择理由,原材料应具有稳定的供货渠道以保证产品质量,需提供原材料生产厂家的资质证明及外购协议。应明确所用原材料的质控标准,提交原材料符合相应标准的全性能验证报告。对于首次应用于该产品的新材料,应提供该材料适合用于人体预期使用部位、预期使用方式的相关研究资料。对于自己研制生产的原材料粒料,应提供详细的配方及研制报告。
(四)生产制造信息
应详细描述该产品的设计过程及生产工艺过程,建议采用流程图的形式表述。详细阐述产品生产工艺过程及其确定依据、质量控制标准及控制措施,标明特殊工艺过程及关键工艺过程的质量控制参数及其对产品物理、化学、机械、生物性能的影响。提交产品工艺稳定性的验证报告。对生产加工过程中所使用的添加剂(辅剂、助剂、粘合剂等)的使用剂量、迁移物的控制措施和标准,提供验证性资料。
医疗器械注册证办理若申报产品有多个研制、生产场地,应概述每个研制、生产场地的概况。
(五)临床评价资料
临床评价资料应按照《医疗器械注册管理办法》提交,并可参考《医疗器械临床评价技术指导原则》选择适合的评价方法,可选择豁免临床目录或者同品种比对的评价方法。申请人应提供不同压力等级对应不同临床作用的临床验证支持性资料。
(六)产品风险分析资料
代办医疗器械注册按照YY/T 0316-2016《医疗器械风险管理对医疗器械的应用》标准的要求,对产品生命周期全过程实施风险管理。申请人在产品准备注册上市前,应对风险管理过程进行评审。评审应至少确保:产品的风险已被全面地分析;风险管理计划已被适当地实施;综合剩余风险是可接受的;已有适当方法获得相关生产和生产后信息。评审结果应形成风险管理报告。风险管理资料应至少包括以下信息:
1.可能影响产品安全性的特征问题清单
医疗器械产品注册证代理应参考YY/T 0316附录C的要求判定医疗器械与安全性有关特征的问题,但识别风险的来源并不局限于此。应对该类产品进行充分的风险识别,风险识别的信息来源需要具体列出,可包括但不局限于以下途径:类似产品的投诉/抱怨数据、医学文献、实验室检测、产品标签标识、专家观点等。对于风险识别信息的来源企业应具体说明,并提交有关支持文件或文献。
2.产品有关危害的清单
应详细列出与产品有关的已知和可预见危害的清单,以及对每个危害如何造成损害的分析(包括可预见的事件序列、危害处境和可能发生的损害)。
应指出拟申报产品所特有的任何额外风险,说明风险分析的方法。已识别的风险应至少包括但不局限于以下方面:
(1)微生物感染产品带有真菌,引起脚气、皮肤瘙痒;
(2)生物相容性危害产品含有致敏材料;生产过程中其他物质带入产品中;使用可分解致癌芳香胺染料;产品使用后处理方式不当;
(3)功能性危害性能与预期用途不相符;货架寿命规定错误造成误用;产品超过有效期;不正确的测试方法;产品损坏;不合适的尺寸规格;使用寿命规定错误造成误用;压力等级达不到要求;压力梯度达不到要求;
(4)使用错误而形成的危害错误的有效期而误用;非预期用途性使用;违背说明书使用;不合理的保养;
(5)使用信息标识错误而形成的危害标签信息不充分、不完整或不适当;不充分或错误的标签信息;不完整的使用说明;不适当的性能描述;
(6)不适当的使用手册预使用检查规范不适当;操作说明书过于复杂;丢失操作手册;不充分的警示信息;副作用警告不充分;禁忌证说明不充分;
应对所识别的风险提出具体的降低风险的措施。降低所申报产品的风险应依据YY/T 0316要求依次从设计、保护、说明书进行考虑。
医疗器械注册证代理应在产品生命全周期中对风险进行管理控制,以使剩余风险在可接受范围内。可通过产品设计控制、产品原材料选择、产品技术性能指标的制定、临床试验、正确的标签标识、灭菌等多项措施以降低风险至可接受水平,但不局限于以上所述。
(七)产品技术要求
产品技术要求应符合《医疗器械产品技术要求编写指导原则》中的相关要求。产品的性能指标应不低于相关的强制性国家标准和行业标准,产品技术要求中的试验方法应有制定依据或为已经过验证的方法。应根据所申报产品特点制定产品技术要求,对宣称的所有技术参数和功能,在产品技术要求中予以规定。
办理医疗器械注册证产品技术要求中应标明产品的规格型号并说明规格型号划分的依据,不使用“主要”、“等”之类模糊词语。产品的性能指标及试验方法,可参考引用YY/T 0851和YY/T 0853作为性能指标和试验方法的选择依据,性能指标一般应至少包括以下内容,并达到GB 18401-2010《国家纺织产品基本安全技术规范》要求。
物理性能:外观、尺寸、压力等级、足跟、接缝、袜边、压缩力系的实现、可伸展性、实际伸展率、比占压力、压缩持久性、松紧度、防滑脱性能、弹性回复率等。
化学性能:纤维鉴别、甲醛含量、酸碱度、色牢度、可分解致癌芳香胺染料等。
医疗器械注册证代理对于采用新材料制造的产品以及具有其他特殊性能的产品,应根据产品特点制定相应的物理、化学、生物性能要求,设计验证该项特殊性能的试验方法,指标的制定依据、试验方法的来源及方法学验证资料应在产品性能研究资料中阐明。
应注意:在说明书中所宣称的可客观判定产品功能性、安全性及与质量控制相关的指标,应在产品技术要求中列出对应的性能要求项目和试验方法。
(八)产品注册检验报告
办理医疗器械注册检验资料应包括注册检验报告及预评价意见。注册检验报告应由具有医疗器械检验资质的检验机构出具,产品在检验机构承检范围内。
所检测型号产品应当是本注册单元内能够代表申报的其他型号产品安全性和有效性的典型产品。应选择结构组成最复杂、所使用的原材料最全面、功能最完全的产品作为典型样品。若型号间的差异可能导致对产品性能和技术特征的影响,应分别选作典型样品。
(九)产品说明书和标签样稿
医疗器械产品注册证代理产品说明书和标签应符合《医疗器械说明书和标签管理规定》的要求及YY/T 0851和YY/T 0853中的相关要求。所提交的文本和标签样图应内容清晰、完整。说明书中所描述的临床适用范围、结构组成、禁忌证、注意事项应与产品的临床资料保持一致。产品的描述、货架有效期应与综述资料和研究资料中所描述及验证的内容一致。应有指导患者选择适当规格型号的原则。此外,还应列明以下内容:
1.操作说明:
袜子的穿脱方法。
袜子的洗涤条件、温度、氯漂、熨烫等信息。
2.注意事项
为了保持卫生,需定期清洗。
需在医生指导下使用。
如遇穿着困难(残疾患者、年龄过大的患者,压力袜太紧等)最佳的解决方法是借助于第三者的帮助。
建议在说明书中可重复使用期限及注意事项,并提交验证报告。
(十)医疗器械注册证有效期内产品分析报告(适用于延续注册)
产品分析报告应能够体现产品在上市期间的市场情况和临床使用情况,应提供以下信息:
所建立的不良事件监测机制及产品随访机制;
产品临床应用情况,用户投诉情况及采取的措施;
医疗器械不良事件汇总分析评价报告,包括产品上市后发生的可疑不良事件列表、说明每一种情况下采取的处理和解决方案,并对上述不良事件进行分析评价,阐明不良事件发生的原因及其对产品安全性、有效性的影响;
在所有国家和地区的产品市场销售情况说明,如销售量,销售单位等。产品型号间差别较大时,应分别提交;
产品监督抽查情况(如有);
若产品上市后发生了召回,应当说明召回的原因、过程和处理结果;
原医疗器械产品注册证中载明要求继续完成工作的,应提供相关总结报告,并附相应资料;
提供上市以来各型号产品的临床回顾分析资料,尤其是随访时间超过1年的临床使用数据。

道和思源(北京)科技有限公司成立于2014年,专注于医疗器械法规咨询服务,致力于为客户将安全、有效和合规的医疗器械产品迅速推向并占领全球市场,是中国领先的医疗器械CRO创新服务企业。主要服务项目有:进口一类医疗器械备案、进口二类医疗器械注册、进口三类医疗器械注册、国产三类医疗器械注册、医疗器械软件注册、临床实验、创新医疗器械申报港澳台医疗器械注册等。
- 上一篇:手术无影灯医疗器械产品注册证申报代办
- 下一篇:医疗器械分类目录
猜你喜欢的内容
- 医用外固定支具2021-07-09
- 02 无源手术器械-04 手术器械钳2020-07-17
- 鹅头钉组合铰刀2021-05-06
- 鼻组织钳2021-06-24
- 金属接骨螺钉2021-04-25
- 医疗器械注册管理办法2020-04-27
- 铜绿假单胞菌和鲍曼不动杆菌敏试剂盒(微量肉汤2021-06-23
- 线锯导引器2021-06-22
- 医用降温贴2021-06-18
- 一次性使用输液器 带针2021-06-23
- 甲状腺手术器械2021-06-24
- 微型腹部外科手术器械2021-05-12
- 软组织环切刀 Tissue Punch2021-04-27
- 手摇式病床2021-04-25
- 牙骨锤 Mallet2021-05-18
- 医疗器械注册证查询2020-07-16

















